Iniciamos un nuevo período...
En este último período trabajaremos las siguientes temáticas:
FLUIDOS EN REPOSO
ü La densidad
ü La presión
ü La presión en los líquidos
ü El principio de Pascal
ü El principio de Arquímedes
ü La presión en los gases
Buen día chicos, por favor enviar al correo la nota de la autoevaluación.
Tener en cuenta:
Buen día, la siguiente información la pueden utilizar como repaso para la evaluación final, les será de gran utilidad para responder las preguntas asociadas en el examen. Por favor ingresar a la plataforma classroom con el siguiente código b456bii, El examen estará habilitado a partir de la 1:00 pm y se cierra el día Domingo 22 de Marzo a la 10:00 pm.
Maquina Térmica:
Una maquina térmica se puede definir como un dispositivo que funciona en un ciclo termodinámico y que realiza cierta cantidad de trabajo neto positivo a través de la transferencia de calor desde un cuerpo a temperatura elevada y hacia un cuerpo a baja temperatura. Con frecuencia el termino maquina térmica se utiliza en un sentido más amplio que incluye a todos los dispositivos que producen trabajo. Entre las que tenemos las maquinas refrigerantes y las bombas de calor. El mejor ejemplo de estas maquinas térmicas son los refrigeradores y bombas de calor que tienen como fin enfriar o calentar un entorno.

Las primeras fuentes de energía utilizadas por las personas fueron los combustibles: madera, carbón, etc. También las primeras máquinas con motor consumían combustibles, como la máquina de vapor desarrollada en el siglo XVIII, que quemaba carbón para mover los pistones. Estos motores son los motores térmicos.
Un motor térmico utiliza la energía almacenada en un combustible y la transforma en movimiento.
Cuando el combustible se quema, la combustión produce gases (vapor de agua u otros). Si el vapor de agua penetra en una cámara cerrada se expandirá ocupando todo el volumen disponible, aumentando la presión. Este aumento de presión hará que un pistón se mueva en el interior de un cilindro. El movimiento del pistón se transmite luego a otras partes móviles de la máquina. Usando un generador, este movimiento también puede convertirse en electricidad.
Los motores térmicos, según la forma de realizar la combustión, pueden ser de dos tipos:
- De combustión externa: el combustible se quema fuera del motor, como en el caso de una máquina de vapor. Por ejemplo, las primeras locomotoras o los barcos de vapor.
- De combustión interna: el combustible se quema dentro de la máquina, como en el motor de un coche.
La máquina de vapor fue la primera máquina capaz de transformar la energía acumulada en un combustible en movimiento de una manera eficiente a escala industrial. La potencia generada por las máquinas de vapor del siglo XVIII era muy superior, por ejemplo, a la que era capaz de desarrollar un molino de viento.
La necesidad que dio origen a la aparición de la máquina de vapor fue la extracción del agua que inundaba muchas minas de carbón en Inglaterra en el siglo XVII. Para extraer el agua se usaban bombas de extracción impulsadas a menudo por caballos, pero este sistema era poco eficiente. Las primeras máquinas de vapor fueron diseñadas por los ingenieros Newcomen y Savery. Luego, otras personas perfeccionaron estas máquinas.
Concretamente fue James Watt (1736-1819) quien consiguió diseñar una máquina bastante eficiente que revolucionó la actividad industrial. La aparición de su máquina de vapor en 1769 marcó una clara frontera en la historia de las máquinas. Este invento fomentó la aparición de máquinas especializadas en la minería, en la industria textil o en los transportes, basadas en combustibles como el carbón, de manera que ya no era necesario que una persona o un animal moviese el mecanismo.
Este hecho transformó por completo la sociedad, pues el tiempo necesario para realizar muchas tareas repetitivas se rebajó apreciablemente. Se produjeron cambios radicales en el modo de vida de las personas: desplazamiento desde las zonas rurales hasta las ciudades, aparición de nuevas profesiones, etc.

Esquema del funcionamiento de una máquina de vapor
El aumento de presión provocado por el calentamiento del agua, que se transforma en vapor, mueve un pistón, el cual, a su vez, hace girar una rueda; el cilindro cuenta con una válvula de salida.
Al quemar combustible se obtiene vapor de agua que recorre un circuito hasta llegar a un cilindro, en el que empuja un pistón que a su vez mueve una rueda. Cuando el pistón alcanza el extremo del cilindro, se abre la válvula de salida, y el pistón vuelve hacia la izquierda empujado por la rueda. Al final de este recorrido del cilindro se cierra la válvula de salida y se vuelve a abrir la válvula de entrada, con lo que el ciclo comienza de nuevo. El efecto final conseguido es el giro continuo de la rueda.

SEGUNDA LEY DE LA TERMODINÁMICA
Al igual que ocurren con otras leyes de termodinámica, el segundo principio es de tipo empírico, llegamos a él a través de la experimentación. La termodinámica no se preocupa de demostrar por qué las cosas son así, y no de otra forma.
La segunda ley de la termodinámica se expresa en varias formulaciones equivalentes:
Enunciado de Kelvin - Planck
No es posible un proceso que convierta todo el calor absorbido en trabajo.
Enunciado de Clausiois
No es posible ningún proceso cuyo único resultado sea la extracción de calor de un cuerpo frío a otro más caliente.
Observa que esta segunda ley no dice que no sea posible la extracción de calor de un foco frío a otro más caliente. Simplemente dice que dicho proceso nunca será espontáneo.
El segundo principio de la termodinámica no se límita exclusivamente a máquinas térmicas sino que se ocupa, en general, de todos los procesos naturales que suceden de manera espontánea. Podemos decir que se ocupa de la evolución natural de los sistemas termodinámicos, es decir, de la dirección en que avanzan. Esta dirección se asocia a la distribución molecular interna de las moléculas.
Para estudiar la espontaneidad de los procesos, el austriaco Ludwig Edward Boltzmann introdujo una nueva magnitud denominada entropía.
La entropía S es una variable de estado. Está asociada a la probabilidad de que un determinado estado ocurra en un sistema. Aquellos más probables tienen una mayor entropía.
Un estudio más exhaustivo de le entropía requiere herramientas matemáticas que están fuera del ámbito de este nivel educativo, sin embargo si es importante que sepas qué relación guarda la entropía con la segunda ley de la termodinámica.
Cualquier proceso natural espontáneo evoluciona hacia un aumento de la entropía.
Veamos algunos ejemplos concretos para entender mejor este concepto:
- Si coges un montón de lápices y los lanzas al aire, cuando caigan es poco probable que caigan alineados. Lo más probable es que caigan en completo desorden
- Si echas azucar al agua, las partículas se distribuyen al azar por toda la disolución de un modo espontáneo, y no en una sola dirección
- En un gas que se expande libremente, la presión en las paredes del recinto en el que se encuentra es la misma en cualquier punto. La razón es que las partículas del gas se han expandido en todas direcciones por igual y no en una en concreto
Vemos pues, que aumento del desorden es la dirección natural en que evolucionan los procesos naturales.
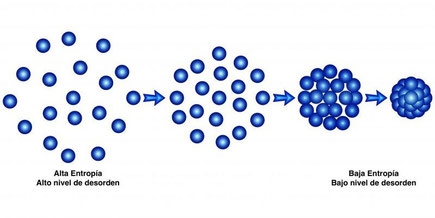
ENTROPÍA
La entropía (S) es una magnitud termodinámica definida originariamente como criterio para predecir la evolución de los sistemas termodinámicos.
La entropía es una función de estado de carácter extensivo. El valor de la entropía, en un sistema aislado, crece en el transcurso de un proceso que se da de forma natural. La entropía describe cómo es de irreversible un sistema termodinámico.
